Sleutelen aan de DNA-code met CRISPR-Cas
De auteursHet nieuwe CRISPR-Cas staat volop in de belangstelling als techniek om genen heel gericht aan te passen. Knippen en plakken dus, met allerlei medische toepassingen of om betere plantgewassen te produceren. Hoe werkt het, wat is er mogelijk, en wat is toegestaan?
De geschiedenis van CRISPR-Cas gaat verder terug dan de paar jaar dat deze techniek in het nieuws komt. Al in 1987 beschreven moleculair bioloog Ishino en zijn collega’s een onbekende DNA-volgorde in bacteriën die zichzelf tekens herhaalde. ‘That’s funny’ was hun eerste reactie. Pas 25 jaar later werden de mogelijke medische toepassingen van ‘Clustered Regularly Interspaced Short Palindromic Repeats-cas’ oftewel CRISPR-Cas voor de eerste keer beschreven in het wetenschappelijke tijdschrift Science. Dit leidde in 2020 tot de Nobelprijs in chemie voor Doudna en Charpentier. Maar wat is CRISPR-Cas nu?
Een ‘schaartje’ om DNA te knippen
CRISPR-Cas is een techniek om DNA aan te passen (Fig. 1). De twee moleculen die onderzoekers hiervoor gebruiken bestaan uit een stukje gids-RNA en een CRISPR-associated protein (Cas) eiwit. Het gids-RNA bestaat uit een 20-tal nucleotiden (letters) die precies gelijk zijn aan de nucleotiden in een stukje DNA dat geknipt moet worden. Het gids-stukje leidt het Cas eiwit naar de juiste plek in het DNA waar het een gen in twee stukken kan knippen net zoals een schaar. De volgorde van de nucleotiden in het gids-stukje is uniek in het DNA, waardoor het CRISPR-Cas maar op één plek in het DNA kan knippen.
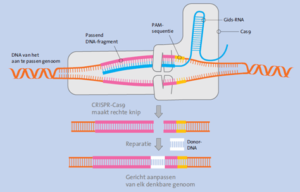
Figuur 1. Schematische weergave van de werking van CRISPR-Cas. Het gids-RNA leidt het eiwit, in dit geval Cas9, naar een unieke plek in het DNA. Het CRISPR-Cas eiwit knipt het DNA in twee stukken. Vervolgens wordt het DNA weer gerepareerd met een extra stukje DNA (donor DNA) en het herstelmechanisme in de cel.
Gene editing
Een cel moet een breuk in het DNA, zoals die door CRISPR-Cas is gemaakt, zo snel mogelijk herstellen om te kunnen overleven. Maar het DNA-herstelmechanisme is slordig en maakt vaak foutjes in de nucleotidenvolgorde. Dankzij die fouten in het DNA kun je bijvoorbeeld een gen uitschakelen. Onderzoekers gebruiken dit om de functie van een gen te onderzoeken of bijvoorbeeld om een Hiv-infectie te remmen. Ook kun je een extra stukje DNA aan de cel geven. De cel gebruikt dit om de breuk te herstellen en zo kun je een gen aanpassen naar wat je maar wilt. Een specifieke verandering inbrengen of een ‘ziek’ gen aanpassen tot een gezonde variant: het behoort allemaal tot de mogelijkheden.
CRISPR-Cas in cel- en diermodellen
CRISPR-Cas wordt meestal gebruikt om nieuwe modellen te maken zoals een (humane) cellijn, gist, worm, fruitvlieg, zebravis, en de muis. Onderzoeker Erwin van Wijk, die oogziekten modelleert in de zebravis zegt hierover: ‘CRISPR-Cas is specifieker, gemakkelijker, sneller, en ook goedkoper dan al langer bestaande technieken om DNA aan te passen. Het is een echte game-changer.’ Ook voor onderzoek naar andere aandoeningen zoals een verstandelijke beperking biedt de techniek voordelen. Tot enkele jaren terug moest je nog een cellijn van de patiënt gebruiken en die vergelijken met gezonde cellijnen. Nu kun je de verandering aanbrengen in dezelfde humane cellijn die je gebruikt als de gezonde controle. Alleen het gen waarin je geïnteresseerd bent wordt hierbij aangepast. Om praktische en ethische redenen is het hiernaast eenvoudiger om onderzoek met een diermodel of humane cellijn te doen, dan onderzoek met mensen.
CRISPR-Cas in de mens: veiligheid voorop
In 2018 werd de wereld opgeschrikt door de Chinese wetenschapper He, die CRISPR-Cas had gebruikt bij de bevruchting om twee baby’s minder gevoelig voor Hiv te maken. De wereld was te klein en sinds dat moment is er een wereldwijde regeling van kracht waarmee het gebruik van de gene-editing technologie in geslachtscellen en embryo’s voor onbepaalde tijd wordt opgeschort.
Maar in volwassenen wordt het gebruik van CRISPR-Cas minder als een probleem gezien. Deng van Peking Universiteit in Beijing heeft eenzelfde soort aanpak gebruikt bij een 27 jaar oude man. Hij had Hiv en leukemie (bloedkanker) waarvoor hij een beenmergtransplantatie nodig had. De wetenschappers hebben beenmergstamcellen van een donor genomen en CRISPR-Cas gebruikt om het CCR5-gen uit zetten waardoor Hiv1 niet meer binnen kan komen in de immuuncellen. Daarna heeft de man een transplantatie ondergaan. Ondanks dat hij nog steeds met Hiv geïnfecteerd is – slechts 5% van zijn immuuncellen zijn aangepast – had hij geen last van bijwerkingen.
Zeer recent zijn ook de eerste succesvolle resultaten gepubliceerd van een op CRISPR-Cas behandeling voor amyloïdose, een erfelijke en levensbedreigende ziekte waarbij verkeerd gevouwen eiwitten neerslaan in met name het hart en zenuwcellen. Ook hier werden geen ernstige bijwerkingen gerapporteerd. Dit soort onderzoeken hebben laten zien dat de techniek nauwkeurig genoeg is om veilig te gebruiken in volwassenen.
Waar gaat het naar toe met CRISPR?
CRISPR is een techniek met steeds bredere toepassingen. Het gids-RNA kan namelijk aangepast worden om elk stukje DNA te herkennen en vervolgens aan te passen. In planten, dieren, en mensen, wordt CRISPR inmiddels ingezet om fundamentele biologische vragen te beantwoorden, medische diagnostiek te doen, nieuwe vormen van behandeling te realiseren, en het produceren van betere gewassen.
Zoals bij elke genetische techniek spelen ook ethische vraagstukken een rol. Een aanpassing van het DNA met CRISPR-Cas leidt immers automatisch tot een genetisch gemodificeerd organisme. Daar zijn echter strenge regels voor. Maar aangezien CRISPR-Cas sneller, eenvoudiger en minder foutgevoelig is, lijkt dit geen probleem voor deze techniek, en kunnen we in de nabije toekomst nog veel nieuwe CRISPR-technieken en toepassingen verwachten.
Nooit meer iets missen?
Wil je altijd op de hoogte blijven van nieuwe boeken, dossiers en lesmaterialen? Schrijf je dan in voor onze nieuwsbrief. Wij sturen je maandelijks een overzicht van alle nieuwe content.