Stikken in de stikstof
De auteursHet is slechts weinig elementen van het periodiek systeem gegeven om tot een crisis te leiden. Meestal is er een tekort: eind jaren 1970 leidden tekorten op de wereldmarkt tot een mondiale zilvercrisis. Bij de stikstofcrisis van nu is er juist sprake van een teveel.
De naam ‘stikstof’ roept onprettige associaties op. Inderdaad, als de lucht uitsluitend uit stikstof zou bestaan, zouden we stikken. Omdat het in werkelijkheid 78 procent is, kunnen we rustig blijven doorademen. Maar in overdrachtelijke zin kunnen we wel degelijk stellen dat we stikken in de stikstof.
Aanwaaien
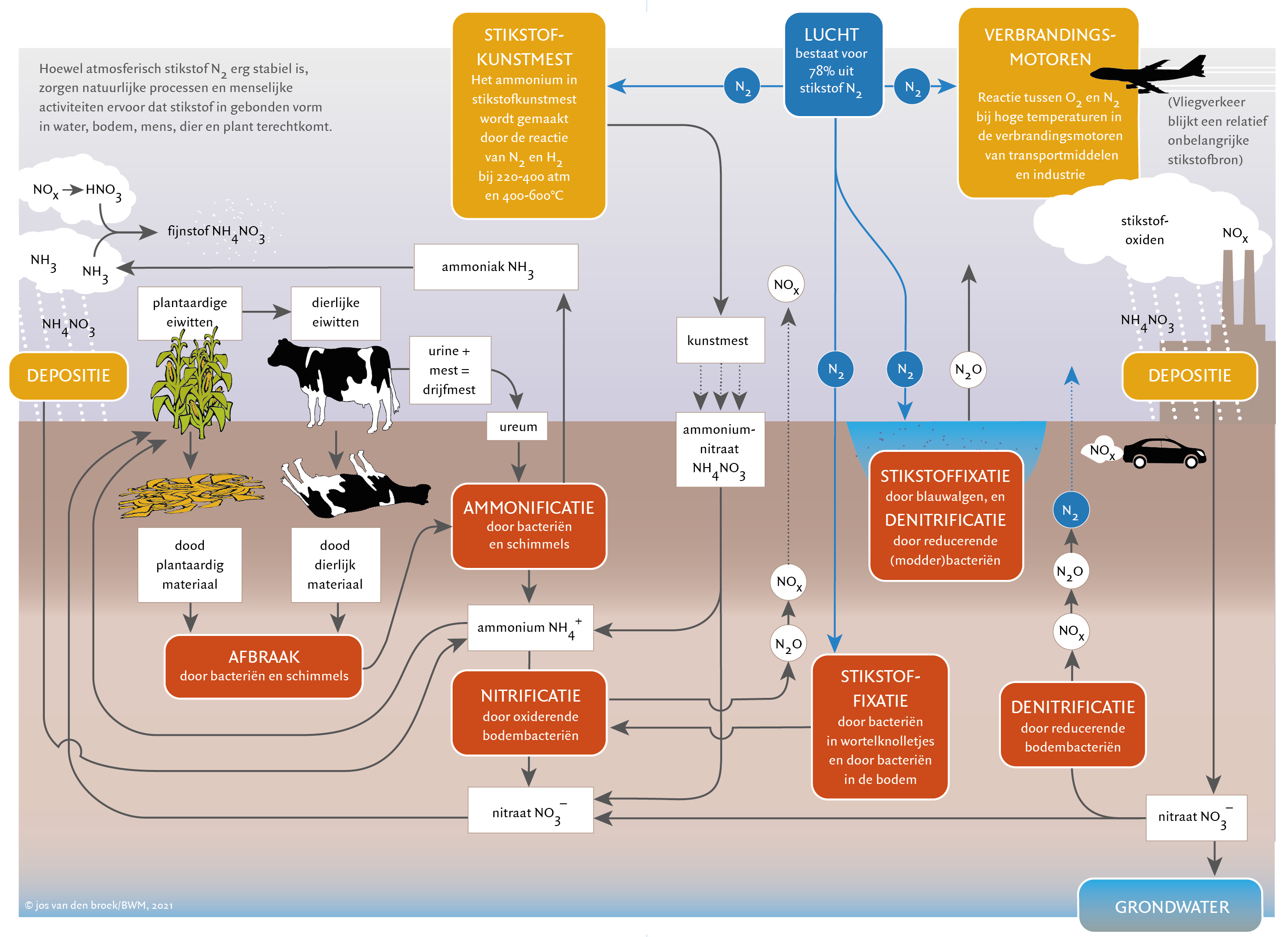
Milieuproblemen door te veel stikstof in bodem en water spelen in de hele wereld, maar in Nederland wel heel sterk. Hier worden bodem en water belast door een zeer hoge toediening van stikstofverbindingen in de landbouw, vooral via dierlijke mest, maar ook via kunstmest. Andere bronnen zijn het verkeer, huishoudens en de industrie.
Menselijke activiteiten waarbij stikstofverbindingen in grote hoeveelheden vrijkomen, schaden ecosystemen op land en in het water. Ze kunnen leiden tot vermindering van de biodiversiteit. Ondanks maatregelen die de emissies van stikstofoxiden en ammoniak al fors hebben teruggebracht, zijn verdergaande emissiereducties noodzakelijk om gevoelige ecosystemen in stand te houden.
Moleculaire K’Nex
Laten we vooropstellen dat stikstof voor al het leven op aarde onontbeerlijk is. Het is een bouwsteen van aminozuren en eiwitten, en voor de erfelijke informatiedragers DNA en RNA. Het speelt ook een grote rol bij de uitwisseling van elektronen en energie in deze moleculen. Zonder stikstof zouden allerlei fysiologische functies niet werken.
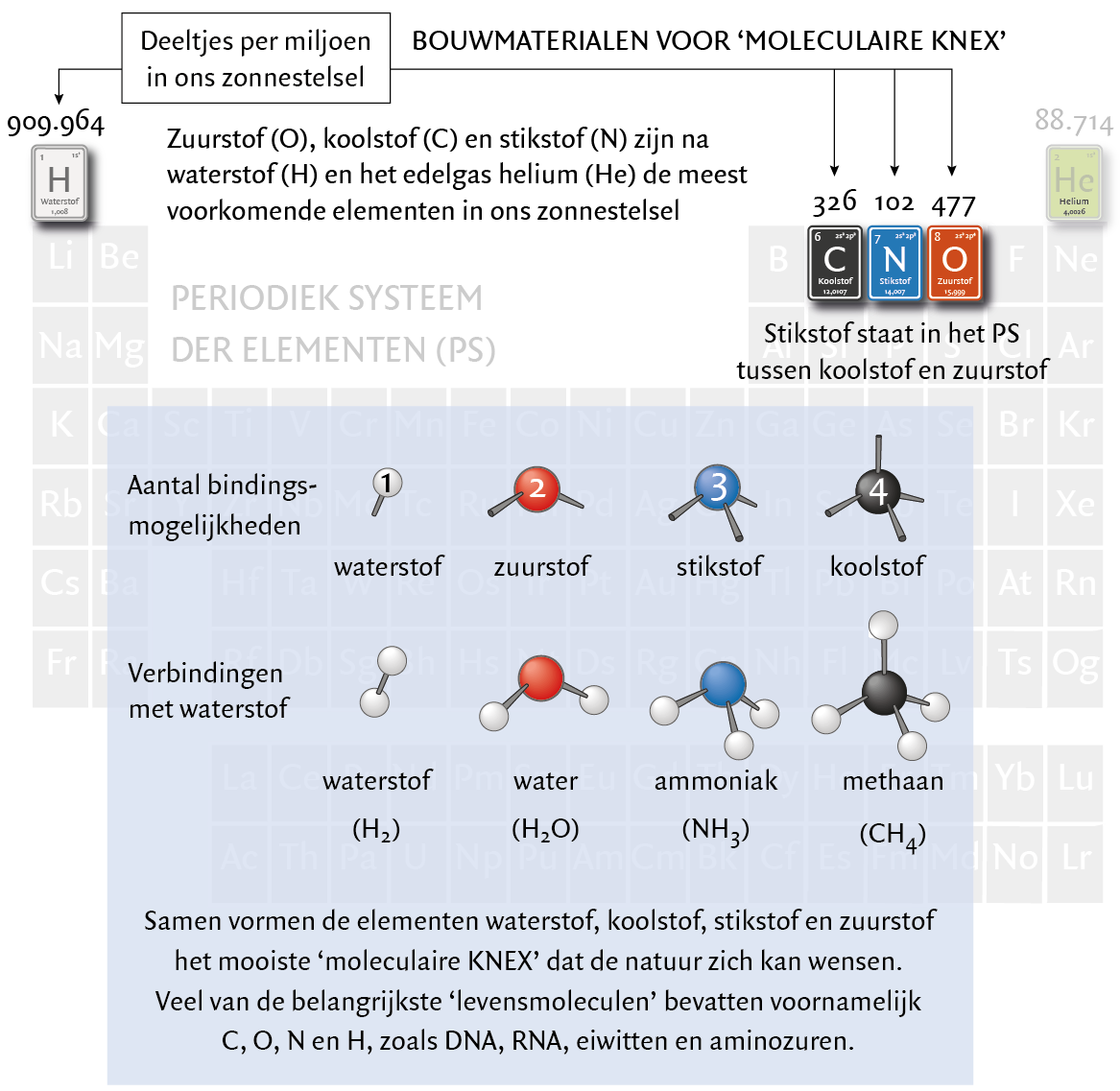
Moleculaire K’Nex-bouwdoos waarin de elementen waterstof (H), koolstof (C), stikstof (N) en zuurstof (O) de boventoon voeren. (©Jos van den Broek)
De natuur heeft gezorgd voor een fascinerende moleculaire K’Nexbouwdoos waarin de elementen waterstof (H), koolstof (C), stikstof (N) en zuurstof (O) de boventoon voeren (zie figuur). Deze elementen nemen de eerste, zesde, zevende en achtste plaats in het periodiek systeem in.
Om te begrijpen waarom juist deze vier elementen ertoe doen, is enige sterrenkundige basiskennis onmisbaar. Letterlijk alles waarvan we zijn gemaakt, was oorspronkelijk sterrenstof. Kort na de oerknal, 13,8 miljard jaar geleden, ontstond uit elementaire deeltjes het oerelement waterstof. Sindsdien worden er sterren geboren doordat materie onder invloed van de zwaartekracht verdicht en samenklontert.
Kernfusie
Wordt in die verdichte klonten de druk hoog genoeg, dan kan waterstof fuseren tot helium (He), het op een na lichtste element. Bij de kernfusie van vier waterstofkernen tot één heliumkern – bestaande uit vier kerndeeltjes – komt straling vrij: zonnestraling!
Sterren bestaan dus voor het overgrote deel uit waterstof en helium, de twee lichtste elementen in de natuur. Vandaar ook dat in het heelal deze twee elementen veruit het meest voorkomen.
Ook helium kan weer fuseren: uit drie kernen ontstaat koolstof, met twaalf kerndeeltjes. Dat kan vervolgens met nog een heliumkern fuseren tot zuurstof, met zestien kerndeeltjes. Ook kan, via een ander, ingewikkelder mechanisme, uit koolstof stikstof ontstaan, dat veertien kerndeeltjes bevat. De basiselementen van onze moleculaire K’Nexbouwdoos komen zo ruimschoots beschikbaar. Wat de bouwdoos zo bijzonder maakt, is het aantal atoombindingen dat de elementen H, O, N en C kunnen aangaan. Ze hebben namelijk respectievelijk één, twee, drie en vier ‘handjes’ waarmee ze zich aan elkaar kunnen koppelen. Al het leven dat we kennen is uit deze elementen opgebouwd.
Motor en bliksem
Een stikstofatoom heeft drie ‘handjes’. Net als waterstof (H2) en zuurstof (O2) komt stikstof in de natuur niet in de vorm van losse atomen voor. Ze vormen twee aan twee een zogeheten distikstofmolecuul (N2), waarin ze elkaar met drie paar ‘handen’ stevig vasthouden. Daardoor reageert N2-gas nauwelijks met andere stoffen – het is behoorlijk inert, zoals dat heet. Alleen bij hoge temperaturen, bijvoorbeeld in verbrandingsmotoren, bij bliksem en bij vulkaanuitbarstingen kan N2 worden geoxideerd tot wat we stikstofoxiden (NOx) noemen: een groep stoffen bestaande uit (vooral) stikstof- en zuurstofatomen. In de vorm van nitraat (NO3¯) belanden ze via regen en sneeuw in bodem en water, waar ze bijdragen aan de stikstofbelasting. Bij de productie van stikstofkunstmest (bijvoorbeeld ammoniumnitraat, NH4NO3) wordt stikstof gebonden aan waterstof onder zeer hoge druk en bij hoge temperatuur.
Ook sommige bacteriën in de bodem en cyanobacteriën of blauwalgen in het water kunnen stikstof binden. De natuur weet zo al vele miljoenen jaren met dat halsstarrige stikstof om te gaan. Andere bodembacteriën kunnen een overmaat aan nitraat juist omzetten in het inerte stikstofgas, waardoor het evenwicht wordt hersteld. Althans, totdat de mens dat ernstig verstoorde.
Nooit meer iets missen?
Wil je altijd op de hoogte blijven van nieuwe boeken, dossiers en lesmaterialen? Schrijf je dan in voor onze nieuwsbrief. Wij sturen je maandelijks een overzicht van alle nieuwe content.